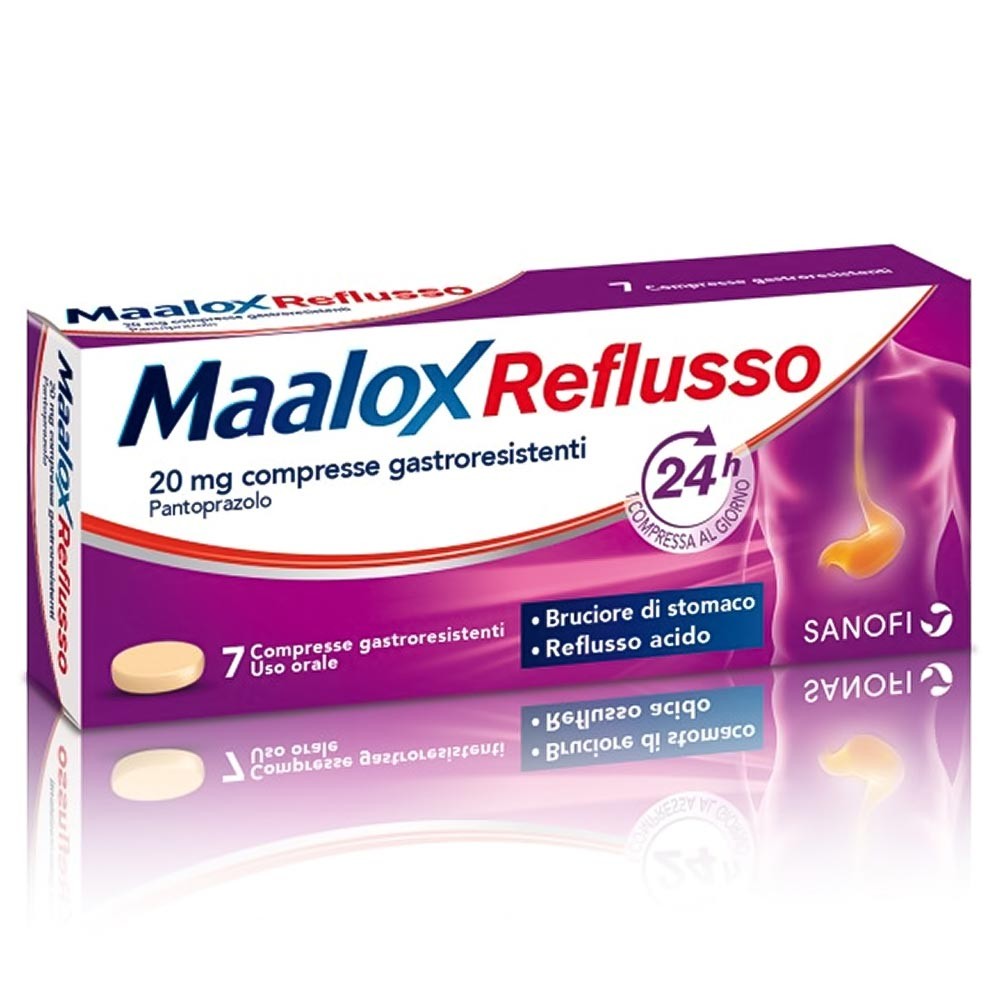
MAALOX REFLUSSO 20 MG 7 COMPRESSE GASTRORESISTENTI

Paga in totale sicurezza con SSL

Spedizioni veloci con corriere

Reso merce disponibile
DENOMINAZIONE:
MAALOX REFLUSSO 20 MG COMPRESSE GASTRORESISTENTI
CATEGORIA FARMACOTERAPEUTICA:
Medicinali per i disturbi correlati alla secrezione acida, inibitori d ella pompa protonica.
PRINCIPI ATTIVI:
Ogni compressa gastroresistente contiene 20 mg di pantoprazolo (come s odio sesquidrato).
Eccipienti con effetti noti: 38,425 mg di maltitolo e 0,345 mg lecitina di soia (derivato dall'olio di soia) e un massimo di 1,84 mg di sodio.
Per l'elenco completo degli eccipienti, vedere p aragrafo 6.1.
ECCIPIENTI:
Nucleo: maltitolo (E965), crospovidone tipo B, sodio carmellosa, sodio carbonato anidro, calcio stearato.
Rivestimento: Poli(vinilalcool), t alco, titanio diossido (E 171), macrogol 3350 lecitina di soia, ferro ossido giallo (E 172), sodio carbonato anidro copolimero acido metacri lico etil acrilato (1:1) (dispersione che contiene polisorbato 80 e so dio laurilsolfato), trietilcitrato.
INDICAZIONI:
Trattamento a breve termine dei sintomi da reflusso (ad es.
pirosi, ri gurgito acido) negli adulti.
CONTROINDICAZIONI/EFF.SECONDAR:
Ipersensibilita' al principio attivo, benzimidazoli sostituiti, alle a rachidi, alla soia o ad uno qualsiasi degli altri eccipienti elencati al paragrafo 6.1.
La contemporanea somministrazione di MAALOX REFLUSSO con gli inibitori della proteasi dell'HIV il cui assorbimento dipende dall'acidita' del pH intragastrico, come atazanavir e nelfinavir, e' controindicata a causa della significativa riduzione della loro biodis ponibilita' (vedere paragrafo 4.5).
(vedere paragrafo 4.5).
POSOLOGIA:
Posologia: la dose raccomandata e' 20 mg di pantoprazolo (una compress a) al giorno.
Potrebbe essere necessario assumere le compresse per 2-3 giorni consecutivi per ottenere un miglioramento dei sintomi.
Una vol ta raggiunta la completa guarigione dei sintomi, il trattamento deve e ssere sospeso.
Il trattamento non deve superare 4 settimane senza cons ultare un medico.
Se entro 2 settimane di trattamento continuo non si nota alcun miglioramento dei sintomi, il paziente deve rivolgersi al m edico.
Popolazioni particolari: non e' necessario l'aggiustamento dell a dose in pazienti anziani o in pazienti con compromissione renale o e patica.
Popolazione pediatrica: l'uso di MAALOX REFLUSSO non e' raccom andato nei bambini e adolescenti al di sotto di 18 anni a causa della insufficienza di dati sulla sicurezza e sull'efficacia.
Modo di sommin istrazione: le compresse gastroresistenti di MAALOX REFLUSSO 20 mg non devono essere masticate o frantumate, e devono essere deglutite inter e con del liquido prima del pasto.
CONSERVAZIONE:
Non conservare a temperatura superiore a 25 gradi C.
AVVERTENZE:
I pazienti devono essere istruiti a rivolgersi al proprio medico se: h anno una perdita di peso non intenzionale, anemia, sanguinamento gastr ointestinale, disfagia, vomito ricorrente o vomito ematico, dal moment o che il trattamento con pantoprazolo puo' alleviare i sintomi e ritar dare la diagnosi di una patologia grave.
In questi casi deve essere es clusa una patologia maligna; hanno avuto precedentemente ulcera gastri ca o chirurgia gastrointestinale; sono in trattamento sintomatico cont inuo per indigestione o per la pirosi da 4 settimane o piu'; hanno itt ero, compromissione epatica, o malattia epatica; hanno qualsiasi altra grave patologia che compromette il benessere generale; hanno piu' di 55 anni con sintomi nuovi o cambiati recentemente.
I pazienti con sint omi ricorrenti relativi a indigestione o pirosi devono consultare il m edico a intervalli regolari.
In particolare, i pazienti con oltre 55 a nni che assumono giornalmente qualsiasi medicinale senza prescrizione per l'indigestione o la pirosi, devono informare il farmacista o il me dico.
I pazienti non devono assumere contemporaneamente un altro inibi tore della pompa protonica o antagonista H 2.
I pazienti che devono es sere sottoposti a endoscopia o test del respiro devono consultare il m edico prima di assumere questo medicinale.
I pazienti devono essere in formati che le compresse non hanno lo scopo di dare un sollievo immedi ato.
I pazienti possono cominciare ad avvertire un miglioramento dei s intomi dopo circa un giorno di trattamento con pantoprazolo, ma potreb be essere necessario assumerlo per 7 giorni per raggiungere un complet o controllo della pirosi.
I pazienti non devono assumere pantoprazolo come farmaco preventivo.
Infezioni gastrointestinali causate da batter i: la riduzione dell'acidita' gastrica, dovuta a qualsiasi motivo, tra cui gli inibitori della pompa protonica, aumenta la conta gastrica de i batteri normalmente presenti nel tratto gastrointestinale.
Il tratta mento con farmaci che riducono l'acidita' provoca un leggero aumento d el rischio di infezioni gastrointestinali come Salmonella, Campylobact er o Clostridium difficile .
Lupus eritematoso cutaneo subacuto (SCLE) : gli inibitori di pompa protonica sono associati con casi molto infre quenti di SCLE.
In caso di lesioni, soprattutto nelle zone della pelle esposte al sole, e se accompagnati da artralgia, il paziente deve riv olgersi ad un medico prontamente e il medico deve prendere in consider azione la sospensione di MAALOX REFLUSSO.
Il lupus eritematoso cutaneo subacuto (SCLE) dopo un precedente trattamento con un inibitore di po mpa protonica puo' aumentare il rischio di SCLE con altri inibitori di pompa protonica.
Lecitina di soia: questo medicinale contiene lecitin a derivata dall'olio di soia.
Se il paziente e' allergico alle arachid i o alla soia, non deve utilizzare questo medicinale.
Maltitolo: quest o medicinale contiene maltitolo.
I pazienti con rari problemi ereditar i d'intolleranza al fruttosio non devono assumere questo medicinale.
S odio: questo medicinale contiene meno di 1 mmol di sodio (23 mg) per c ompressa, cioe' e' essenzialmente "senza sodio".
Interferenza con esam i di laboratorio: un livello aumentato di Cromogranina A (CgA) puo' in terferire con gli esami diagnostici per tumori neuroendocrini.
Per evi tare tale interferenza, il trattamento con MAALOX REFLUSSO deve essere sospeso per almeno 5 giorni prima delle misurazioni della CgA (vedere paragrafo 5.1).
Se i livelli di CgA e di gastrina non sono tornati en tro il range di riferimento dopo la misurazione iniziale, occorre ripe tere le misurazioni 14 giorni dopo l'interruzione del trattamento con inibitore della pompa protonica.
Questo medicinale e' destinato esclus ivamente ad un uso a breve termine (fino a 4 settimane) (fare riferime nto al paragrafo 4.2).
I pazienti devono essere avvertiti dei rischi a ggiuntivi con l'uso del medicinale a lungo termine e occorre sottoline are la necessita' della prescrizione e di un monitoraggio periodico.
I seguenti rischi aggiuntivi sono considerati rilevanti in un trattamen to a lungo termine.
Influenza sull'assorbimento della vitamina B12: pa ntoprazolo, come tutti i medicinali acido- bloccanti, puo' ridurre l'a ssorbimento della vitamina B12 (cianocobalamina) a causa di ipo- o acl oridria.
Questo deve essere considerato nei pazienti con riserve corpo ree ridotte o fattori di rischio per ridotto assorbimento della vitami na B12 nella terapia a lungo termine o se si osservano i relativi sint omi.
Fratture ossee: gli inibitori di pompa protonica, specialmente se utilizzati a dosaggi elevati e per periodi prolungati (> 1 anno), pos sono aumentare lievemente il rischio di fratture dell'anca, del polso e della colonna vertebrale, soprattutto nella popolazione anziana o in presenza di altri fattori di rischio riconosciuti.
Studi osservaziona li suggeriscono che gli inibitori di pompa protonica possono aumentare il rischio complessivo di fratture del 10-40%.
Tale aumento potrebbe essere in parte dovuto ad altri fattori di rischio.
I pazienti a risch io di osteoporosi devono ricevere cure basate sulle attuali linee guid a cliniche e devono assumere un'adeguata quantita' di vitamina D e cal cio.
Ipomagnesemia: in pazienti trattati con PPI come pantoprazolo per almeno 3 mesi e, in molti casi per i pazienti trattati per un anno, e ' stata segnalata la presenza di ipomagnesemia grave.
Si possono verif icare serie manifestazioni di ipomagnesiemia come affaticamento, tetan ia, delirio, convulsioni, capogiri e aritmia ventricolare, che potrebb ero insorgere in modo subdolo ed essere sottovalutati.
Nella maggior p arte dei pazienti, l'ipomagnesemia migliora dopo la reintegrazione del le riserve di magnesio e la sospensione del PPI.
Per i pazienti per i quali e' previsto un trattamento prolungato con PPI o in associazione a digossina o medicinali che possono causare ipomagnesemia (ad esempio diuretici), gli operatori sanitari dovrebbero considerare la misurazi one dei livelli di magnesio prima di iniziare il trattamento con PPI e periodicamente durante il trattamento.
INTERAZIONI:
Effetto di pantoprazolo sull'assorbimento degli altri medicinali: MAAL OX REFLUSSO puo' ridurre l'assorbimento dei principi attivi la cui bio disponibilita' dipende dal pH gastrico (ad es.
ketoconazolo).
Inibitor i della proteasi dell'HIV: la co-somministrazione di pantoprazolo con inibitori della proteasi dell'HIV, come atazanavir e nelfinavir il cui assorbimento dipende dall'acidita' del pH intragastrico, e' controind icata a causa della significativa riduzione della loro biodisponibilit a' (vedere paragrafo 4.3).
Anticoagulanti cumarinici (fenprocumone o w arfarin): sebbene negli studi clinici di farmacocinetica non sono stat e osservate interazioni durante il trattamento concomitante con fenpro cumone o warfarin, alcuni casi isolati di variazione dell'Internationa l Normalised Ratio (INR) sono stati segnalati durante il trattamento c oncomitante nel periodo post-marketing.
Quindi, nei pazienti trattati con anticoagulanti cumarinici (ad es.
fenprocumone o warfarin), si rac comanda di monitorare il tempo di protrombina/INR quando si inizia il trattamento con pantoprazolo, quando si interrompe o quando viene somm inistrato in maniera discontinua.
Metotressato: in alcuni pazienti, e' stato segnalato che l'uso concomitante di metotressato ad alto dosagg io (ad es.
300 mg) e inibitori della pompa protonica aumenta i livelli di metotressato.
Pertanto, nei casi in cui il metotressato viene util izzato ad alto dosaggio, per esempio nel trattamento di tumori e della psoriasi, deve essere valutata una sospensione temporanea della terap ia con pantoprazolo.
Altri studi di interazione: il pantoprazolo e' me tabolizzato nel fegato dal sistema enzimatico del citocromo P450.
Stud i di interazione con carbamazepina, caffeina, diazepam, diclofenac, di gossina, etanolo, glibenclamide, metoprololo, naprossene, nifedipina, fenitoina, piroxicam, teofillina e un contraccettivo orale contenente levonorgestrel ed etinilestradiolo non hanno evidenziato interazioni c linicamente significative.
In ogni caso non puo' essere esclusa una in terazione del pantoprazolo con altre sostanze che vengono metabolizzat e dallo stesso sistema enzimatico.
Non ci sono state interazioni con a ntiacidi somministrati contemporaneamente.
EFFETTI INDESIDERATI:
Riassunto del profilo di sicurezza: ci si puo' aspettare che circa il 5% dei pazienti manifesti reazioni avverse.
Le reazioni avverse piu' c omunemente riportate sono diarrea e mal di testa, entrambe verificates i in circa l'1% dei pazienti.
Elenco delle reazioni avverse: le seguen ti reazioni avverse sono state osservate con pantoprazolo.
All'interno del seguente elenco, le reazioni avverse sono classificate in base al la classificazione di frequenza MedRA: molto comune (>=1/10); comune ( >=1/100, <1/10); non comune (>=1/1000, <1/100); raro (>=1/10.000, <1/1 000); molto raro (<1/10.000), non nota (la frequenza non puo' essere d efinita sulla base dei dati disponibili).
All'interno di ciascuna clas se di frequenza, le reazioni avverse sono riportate in ordine decresce nte di gravita'.
Reazioni avverse con pantoprazolo negli studi clinici e nell'esperienza post-marketing.
Patologie del sistema emolinfopoiet ico.
Raro: agranulocitosi; molto raro: trombocitopenia; leucopenia, pa ncitopenia.
Disturbi del sistema immunitario.
Raro: ipersensibilita' ( incluse reazioni anafilattiche e shock anafilattico); disturbi del met abolismo e della nutrizione.
Raro: iperlipidemie e aumento dei lipidi (trigliceridi, colesterolo); variazioni di peso; non nota: iponatriemi a, ipomagnesiemia ipocalcemia in associazione a ipomagnesemia.
Disturb i psichiatrici.
Non comune: disturbi del sonno; raro: depressione (e t utte le forme aggravate); molto raro: disorientamento (e tutte le form e aggravate); non nota: allucinazioni; confusione (specialmente in paz ienti predisposti, cosi' come l'aggravamento di questi eventi in caso di pre-esistenza).
Patologie del sistema nervoso.
Non comune: mal di t esta; capogiri; raro: disturbi del gusto; non nota: parestesia.
Patolo gie dell'occhio.
Raro: disturbi della visione/visione offuscata.
Patol ogie gastrointestinali.
Comune: polipi della ghiandola fundica (benign i); non comune: diarrea; nausea/vomito; distensione addominale e gonfi ore; stitichezza; bocca secca; dolore e disturbi addominali; non nota: colite microscopica.
Patologie epatobiliari.
Non comune: aumento dei livelli degli enzimi epatici (transaminasi, gamma-gt); raro: aumento d ella bilirubina; non nota: lesione epatocellulare; ittero; insufficien za epatocellulare.
Patologie della cute e del tessuto sottocutaneo.
No n comune: eruzione cutanea/esantema/eruzione; prurito; raro: orticaria ; angioedema; non nota: sindrome di steven-johnson; sindrome di lyell; eritema multiforme; fotosensibilita' lupus eritematoso cutaneo subacu to (vedere paragrafo 4.4).
Patologie del sistema muscoloscheletrico e del tessuto connettivo.
Non comune: fratture del polso, dell'anca e de lla colonna vertebrale; raro: artralgia; mialgia.
Patologie renali e u rinarie.
Non nota: nefrite interstiziale.
Patologie dell'apparato ripr oduttivo e della mammella.
Raro: ginecomastia.
Patologie sistemiche e condizioni relative alla sede di somministrazione.
Non comune: astenia , affaticamento e malessere; raro: aumento della temperatura corporea; edema periferico.
Segnalazione delle reazioni avverse sospette.
La se gnalazione delle reazioni avverse sospette che si verificano dopo l'au torizzazione del medicinale e' importante, in quanto permette un monit oraggio continuo del rapporto beneficio/rischio del medicinale.
Agli o peratori sanitari e' richiesto di segnalare qualsiasi reazione avversa sospetta tramite il sistema nazionale di segnalazione all'indirizzo: www.agenziafarmaco.gov.it/it/responsabili.
http://www.aifa.gov.it/cont ent/segnalazioni-reazioni- avverse.
GRAVIDANZA E ALLATTAMENTO:
Gravidanza: non vi sono dati adeguati riguardanti l'uso del pantoprazo lo in donne in gravidanza.
Gli studi condotti sugli animali hanno evid enziato una tossicita' riproduttiva.
Studi preclinici non hanno eviden ziato compromissione della fertilita' o effetti teratogeni (vedere par agrafo 5.3).
Il rischio potenziale per gli esseri umani non e' noto.
M AALOX REFLUSSO non deve essere usato durante la gravidanza.
Allattamen to: e' stata individuata nel latte materno la presenza di pantoprazolo /metaboliti.
L'effetto di pantoprazolo sui neonati/lattanti non e' not o.
MAALOX REFLUSSO non deve essere usato durante l'allattamento al sen o.
Fertilita': non c'e' stata evidenza di ridotta fertilita' in seguit o alla somministrazione di pantoprazolo negli studi sugli animali (ved ere paragrafo 5.3).